
A vese primer szoliter fibrÃģzus tumora: esettanulmÃĄny ÃĐs irodalmi ÃĄttekintÃĐs
CÃĐlkitÅązÃĐs: A szerzÅk ritka, veseeredetÅą fibrÃģzus tumor esetÃĐt mutatjÃĄk be ÃĄttekintve az irodalmi hÃĄtteret is.
EsetismertetÃĐs: A szoliter fibrÃģzus tumor (SFT) egy ritka mesenchymalis daganat, amely elsÅsorban a pleurÃĄban fordul elÅ. Primeren a vesÃĐbÅl kiindulva extrÃĐm ritkÃĄn kerÞl felfedezÃĐsre. Az esettanulmÃĄnyunkban szereplÅ 21 ÃĐves fÃĐrfi pÃĄciens kivizsgÃĄlÃĄsa ismÃĐtlÅdÅ, tudatzavarokkal is jÃĄrÃģ hypoglykaemiÃĄs epizÃģdok miatt indult, amely sorÃĄn felfedezÃĐsre kerÞlt jobb oldali vesetumora. A kezdeti core biopszÃĄs mintavÃĐtel diagnosztikus dilemmÃĄt okozott, de a kÃĐsÅbbi radikÃĄlis nephrectomiÃĄbÃģl szÃĄrmazÃģ specimen immunhisztokÃĐmiai vizsgÃĄlata igazolta a vese primer szoliter fibrÃģzus tumorÃĄt. BetegÞnk mÅątÃĐtet kÃķvetÅ hÃĄromhÃģnapos utÃĄnkÃķvetÃĐse alkalmÃĄval ezidÃĄig sem recidÃva, sem metasztÃĄzis nem igazolÃģdott.
MegbeszÃĐlÃĐs: A kezelÃĐsÃĐnek alapja elsÅdlegesen sebÃĐszi, amely ÃĄttÃĐtes esetben magÃĄban foglalja a metastasectomiÃĄt is. Tekintettel a recidÃva ÃĐs a tÃĄvoli ÃĄttÃĐtkÃĐpzÃĐs lehetÅsÃĐgÃĐre, gondos utÃĄnkÃķvetÃĐs ajÃĄnlott.
BevezetÃĐs
A szoliter fibrÃģzus tumor â korÃĄbbi nevÃĐn hemangiopericytoma â egy ritka mesenchymalis daganat, amely a szervezetben szÃĄmos lokalizÃĄciÃģban elÅfordulhat (1). ElsÅkÃĐnt a pleurÃĄban Ãrta le Klemperer ÃĐs Rabin 1931-ben, de szinte bÃĄrhonnan kiindulhat (2). VÃĄltozatos elÅfordulÃĄsi helyei kÃķzÃķtt emlÃtendÅ a peritoneum, pericardium, agyhÃĄrtya, gerincvelÅ, hasnyÃĄlmirigy (3), mÃĄj (4), de leÃrtÃĄk szublingvÃĄlis nyÃĄlmirigyben [5] , vagy intraocularisan (6) is.
Az immunhisztokÃĐmia ÃĐs a molekulÃĄris diagnosztika fejlÅdÃĐsÃĐvel a CD34 vÃĄlt a szoliter fibrÃģzus tumor leginkÃĄbb jellemzÅ markerÃĐvÃĐ, habÃĄr ez sem bizonyult teljesen specifikusnak a tumortÃpus pontos identifikÃĄciÃģjÃĄban. Napjainkra a NAB2-STAT6 fÚziÃģs gÃĐn felfedezÃĐse az SFT mÃĐg pontosabb diagnosztikÃĄjÃĄt teszi lehetÅvÃĐ (2).
A szoliter fibrÃģzus tumorok nagy rÃĐsze benignus, kevesebb, mint 20%-ban azonban malignus daganatkÃĐnt viselkedve lokÃĄlisan invazÃv ÃĐs metasztÃĄzist kÃĐpez (7).
Az SFT elsÅdleges kezelÃĐse a negatÃv sebÃĐszi szÃĐllel tÃķrtÃĐnÅ kimetszÃĐs, de mÃĐg radikÃĄlis excÃziÃģ mellett is szoros utÃĄnkÃķvetÃĐs javasolt a lokÃĄlis recidÃva lehetÅsÃĐge miatt (8). A sugÃĄr- ÃĐs kemoterÃĄpia nem kellÅen hatÃĐkony, Ãgy a standard kezelÃĐsnek nem rÃĐsze, ÃĄm szelektÃĄlt esetekben â multidiszciplinÃĄris dÃķntÃĐst kÃķvetÅen â egyÃĐnre szabott terÃĄpiÃĄs stratÃĐgiÃĄk is megfontolhatÃģak (2).
EsetismertetÃĐs
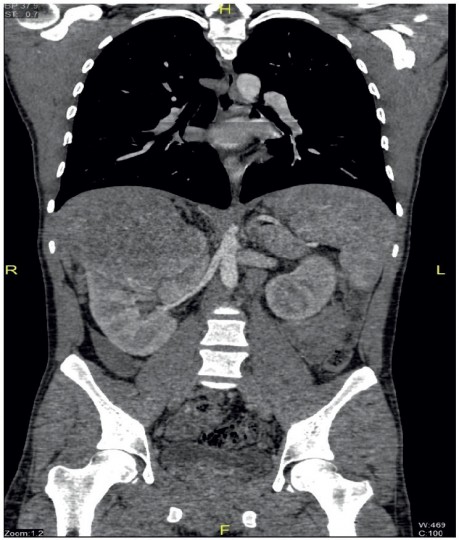
21 ÃĐves fÃĐrfi pÃĄciensÞnk tÃĄvolabbi kÃģrelÅzmÃĐnyÃĐben mindÃķssze egy gyermekkori lÃĄgyÃĐksÃĐrvmÅątÃĐt szerepel. Egy kÃķnnyÅązenei fesztivÃĄlrÃģl alkoholos intoxikÃĄciÃģ gyanÚjÃĄval a SiÃģfoki KÃģrhÃĄz IntenzÃv OsztÃĄlyÃĄra kerÞlt felvÃĐtelre, ahol ÃĐszlelÃĐse sorÃĄn tÃķbbszÃķr vÃĄlt hypoglykaemiÃĄssÃĄ, agresszÃv viselkedÃĐse miatt szedatÃvumokra szorult. BelgyÃģgyÃĄszati kivizsgÃĄlÃĄsa alkalmÃĄval felfedezÃĐsre kerÞlt jobb oldali vesedaganata (1. ÃĄbra).
A tÃĐrfoglalÃĄsbÃģl core biopsziÃĄs mintavÃĐtel tÃķrtÃĐnt, amely alapjÃĄn low grade mesenchymalis daganat (fibromyxoid sarcoma variÃĄns) lehetÅsÃĐge merÞlt fel, Ãgy radikÃĄlis nephrectomiÃĄt vÃĐgeztÞnk.
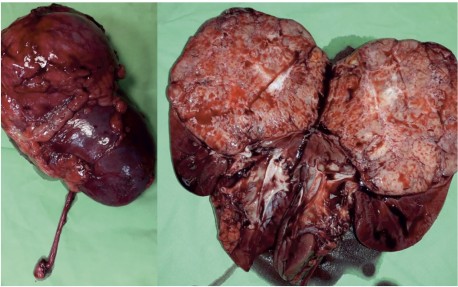
MakroszkÃģposan az eltÃĄvolÃtott ÃĐs hilusi oldalÃĄn felvÃĄgott vese felsÅ ÃĐs kÃķzÃĐpsÅ harmadÃĄt tejesen ÃĐs az alsÃģ harmadÃĄt rÃĐszben kitÃķltÅ 11,5 cm à 10 cm à 8 cm nagysÃĄgÚ, jÃģl kÃķrÞlÃrt, dominÃĄnsan szÞrkÃĐsfehÃĐr, nÃĐhol sÃĄrgÃĄsfehÃĐr tumort lÃĄttunk, amely centrumÃĄban pÃģkhÃĄlÃģszerÅą rajzolatot mutatott. Szabad szemmel vizsgÃĄlva a daganat a vese pyelonjÃĄt ÃĐs hilusÃĄt deformÃĄlta, de sem az Þregrendszerbe, sem pedig a rostos tokba valÃģ betÃķrÃĐs nem lÃĄtszott (2. ÃĄbra).
MikroszkÃģposan a mesenchymalis jellegÅą tumorsejtek mellett myxoid ÃĐs fibrotikus gÃģcok ÃĐs kisebb-nagyobb nekrotikus terÞletek is megfigyelhetÅek voltak.
A veseÃĄllomÃĄnyra lokalizÃĄlt tumor szÃĐlÃĐn tÃķbbnyire tokszerÅą kÃķtÅszÃķvet hÚzÃģdott, de helyenkÃĐnt ez hiÃĄnyzott, fÅleg a pyelon felÃĐ esÅ terÞleteken. Nagy nagyÃtÃĄssal elszÃģrtan megfigyelhetÅ volt ezen tokszerÅą struktÚra infiltrÃĄciÃģja. A hilusi kÃĐpleteknek megfelelÅen tumorterjedÃĐs nem volt lÃĄthatÃģ, egyetlen aprÃģ reaktÃv nyirokcsomÃģ ÃĄbrÃĄzolÃģdott.
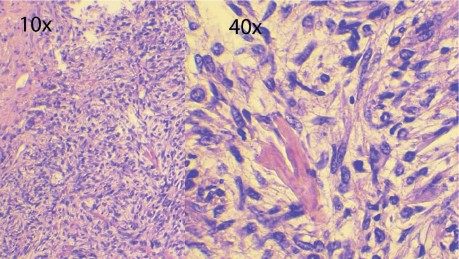
Az elvÃĐgzett immunhisztokÃĐmiai vizsgÃĄlatok sorÃĄn bÃĄr az SFT-re jellemzÅ CD34-immunreakciÃģ negatÃv volt, de a STAT5-reakciÃģ pozitivitÃĄsa szoliter fibrÃģzus tumort igazolt ÃĐs a low grade fibromyxoid sarcoma kizÃĄrÃĄsra kerÞlt (3. ÃĄbra).
BÃĄr a lÃĄtott szÃķveti kÃĐp a malignitÃĄs kritÃĐriumait teljes egÃĐszÃĐben nem elÃĐgÃtette ki, tekintettel a tumor nagy mÃĐretÃĐre, a fokÃĄlisan emelkedett mitotikus aktivitÃĄsra, a daganat hatÃĄrÃĄn nÃĐhol megfigyelhetÅ infiltratÃv nÃķvekedÃĐsi jellegre, a szokatlan CD34-negativitÃĄsra ÃĐs a fokÃĄlis p53-pozitivitÃĄsra a patolÃģgiai lelet onkolÃģgiai kÃķvetÃĐst javasolt.
MegbeszÃĐlÃĐs
Az angol nyelvÅą irodalomban 2019. februÃĄrig a PubMed adatbÃĄzisÃĄban (https://www.ncbi.nlm.nih.gov/pubmed/) a âsolitary fibrous tumorâ, a âkidneyâ ÃĐs a ârenalâ keresÅszavak kombinÃĄciÃģit hasznÃĄlva 78 darab primeren a vesÃĐbÅl kiindulÃģ szoliter fibrÃģzus tumoros esetet azonosÃtottunk. Szinte kivÃĐtel nÃĐlkÞl elsÅ terÃĄpiÃĄs lÃĐpÃĐskÃĐnt sebÃĐszeti beavatkozÃĄs tÃķrtÃĐnt, amely tÃķbbnyire radikÃĄlis nephrectomia volt, de tÃķbb tumorreszekciÃģ ÃĐs egy nephro-ureterectomia is kÃķzlÃĐsre kerÞlt (9).
10 esetben szoliter vagy multiplex metasztÃĄzist is dokumentÃĄltak (az Ãķsszes eset 13%-a). A metasztÃĄzisok leggyakrabban a mÃĄjban (6 esetben) ÃĐs a tÞdÅben (5 esetben) kerÞltek leÃrÃĄsra, de elÅfordult nyirokcsomÃģ (2 eset), csont (2 eset), peritoneum (10) (1 eset), pleura (11) (1 eset), pancreas (12)
(1 eset), ÃĐs ellenoldali veseÃĄttÃĐt is (13) (1 eset), amely radikÃĄlis nephrectomiÃĄt kÃķvetÅen 8 ÃĐvvel kÃĐsÅbb alakult ki kontralaterÃĄlisan.
SzÃĄmos kÃķzlemÃĐnyben a metasztÃĄzisok a primer vesetumorral szimultÃĄn kerÞltek sebÃĐszi eltÃĄvolÃtÃĄsra, Ãķsszesen nÃĐgy mÃĄjreszekciÃģ, egy tÞdÅreszekciÃģ (14), egy pancreas-reszekciÃģ, egy ellenoldali vesereszekciÃģ ÃĐs egy peritonealis metastasectomia kerÞlt leÃrÃĄsra.
Az SFT kezelÃĐsÃĐben a vilÃĄgon elsÅkÃĐnt egy kolumbiai esettanulmÃĄny adjuvÃĄns interferon-alfa-2b hasznÃĄlatÃĄt dokumentÃĄlta egy tÞdÅ- ÃĐs pleurÃĄlis ÃĄttÃĐtekkel rendelkezÅ pÃĄciens kezelÃĐsÃĐnÃĐl ÃĐs a betegsÃĐget progressziÃģmentesnek Ãrta le 23 hÃģnappal kÃĐsÅbbi utÃĄnkÃķvetÃĐs alkalmÃĄval (11).
Egy esetben a sebÃĐszi eltÃĄvolÃtÃĄs helyett a vesedaganat obszervÃĄciÃģjÃĄt vÃĐgeztÃĐk, amely egyÃĐves utÃĄnkÃķvetÃĐs alkalmÃĄval progressziÃģt nem mutatott (15).
KÃĐt kÃķzlemÃĐnyben kerÞlt bemutatÃĄsra lokÃĄlrecidÃva a veseÃĄgyban nephrectomiÃĄt kÃķvetÅen (16, 17), mindkÃĐt alkalommal a recidÃva ismÃĐtelt sebÃĐszi eltÃĄvolÃtÃĄsÃĄra kerÞlt sor.
Egy esetben kÃĐtoldali vese SFT kerÞlt kÃķzlÃĐsre (18), egyszer egy mindÃķssze 3 ÃĐves gyermekben ÃrtÃĄk le (19), egy alkalommal pedig â kÃķzlemÃĐnyÞnkhÃķz hasonlÃģan â hypoglykaemia, mint paraneoplÃĄziÃĄs tÞnet vezetett a vese szoliter fibrÃģzus tumorÃĄnak felismerÃĐsÃĐhez (20). E kÃķzlemÃĐnyben a visszatÃĐrÅ alacsony vÃĐrcukorszintek hÃĄtterÃĐben a daganat ÃĄltal kÃĐpzett, az inzulinnal nagyfokÚ strukturÃĄlis ÃĐs biokÃĐmiai homolÃģgiÃĄt mutatÃģ IGF-2 (insulin-like growth factor-2) ÃĄllt, amelynek emelkedett szÃĐrumszintje a tumor reszekciÃģjÃĄt kÃķvetÅen normalizÃĄlÃģdott ÃĐs a hypoglykaemiÃĄs epizÃģdok megszÅąntek.
KÃķvetkeztetÃĐsek
A vese szoliter fibrÃģzus tumora ritkÃĄn fordul elÅ ÃĐs bÃĄr tÃķbbnyire benignus viselkedÃĐsÅą, nem extrÃĐm ritka a metasztÃĄzisok, illetve a lokÃĄlrecidÃva kialakulÃĄsa sem. KezelÃĐsÃĐnek alapja elsÅdlegesen sebÃĐszi, amely ÃĄttÃĐtes esetben magÃĄban foglalja a metastasectomiÃĄt is. Tekintettel a recidÃva ÃĐs a tÃĄvoli ÃĄttÃĐtkÃĐpzÃĐs lehetÅsÃĐgÃĐre â akÃĄr ÃĐvekkel kÃĐsÅbb is â gondos utÃĄnkÃķvetÃĐs ajÃĄnlott.
2. Brian Davanzo, Robert E. Emerson, Megan Lisy. Solitary fibrous tumor. Transl Gastroenterol Hepatol. 2018 Nov 21; 3: 94. DOI: 10.21037/tgh.2018.11.02
3. DâAmico FE, Ruffolo C, Romano M et al. Rare neoplasm mimicking neuoroendocrine pancreatic tumor: A case report of solitary fibrous tumor with review of the literature. Anticancer Res 2017; 37: 3093â3097. DOI: 10.21873/anticanres.11665
4. Sun Z, Ding Y, Jiang Y, et al. Ex situ hepatectomy and liver autotransplantation for a treating giant solitary fibrous tumor: A case report ONCOLOGY LETTERS 2019; 17: 1042â1052. DOI: 10.3892/ol.2018.9693
5. Iorio B, Ronchi A, Montella M, et al. Malignant extrapleural solitary fibrous tumor arising in the sublingual gland: A case report and review of literature. Oral Oncol 2019 Jan 9. pii: S1368â8375 (18) 30476â7. DOI: 10.1016/j.oraloncology.2018.12.013
6. Rinaldo L, Xu SCY, Eggers SD, et al. Rare Occurrence of an Intraocular Choroidal Solitary Fibrous Tumor/Hemangiopericytoma. Ocul Oncol Pathol 2018 Jun; 4(4): 213â219. DOI: 10.1159/000481947
7. Robinson LA. Solitary fibrous tumor of the pleura. Cancer Control 2006; 13: 264â269. DOI: 10.1177/107327480601300403
8. Thway K, Ng W, Noujaim J, et al. The current status of solitary fibrous tumor: diagnostic features, variants, and genetics. Int J Surg Pathol 2016; 24(4): 281â92. DOI: 10.1177/1066896915627485
9. Guo G, Zhang X, Zhou ZH, et al. Clinical characteristics of malignant solitary fibrous tumors of the kidney with thoracic vertebral metastasis. Int J Urol 2012 Feb; 19(2): 177â8. DOI: 10.1111/j.1442â2042.2011.02921.x
10. RodrÃguez Cruz, HernÃĄndez SÃĄnchez, BlÃĄzquez, et al. Malignant solitary fibrous kidney tumor with peritoneal disease: a case report. Case Rep Nephrol Urol 2014 Apr 11; 4(1): 70â4. DOI: 10.1159/000362539
11. Cuello J, BrugÃĐs R. Malignant solitary fibrous tumor of the kidney: report of the first case managed with interferon. Case Rep Oncol Med 2013; 2013: 564980. DOI: 10.1155/2013/564980
12. Patel YA, Dhalla S, Olson MT, et al. Pancreatic metastasis from a solitary fibrous tumor of the kidney: a rare cause of acute recurrent pancreatitis. Pancreatology 2013 Nov-Dec; 13(6): 631â3. DOI: 10.1016/j.pan.2013.06.004
13. Cheung, Talanki, Liu, et al. Metachronous Malignant Solitary Fibrous Tumor of Kidney: Case Report and Review of Literature. Urol Case Rep 2015 Oct 17; 4: 45â7. DOI: 10.1016/j.eucr.2015.09.004
14. Sasaki, Kurihara T, Katsuoka Y, et al. Distant metastasis from benign solitary fibrous tumor of the kidney. Case Rep Nephrol Urol 2013 Jan; 3(1): 1â8. DOI: 10.1159/000346850
15. Petrella F, Monfardini L, Musi G, et al. Synchronous pleuro â renal solitary fibrous tumors: a new clinical-pathological finding. Minerva Chir 2009 Dec; 64(6): 669â71.
16. Usuba W, Sasaki H, Yoshie H, et al. Solitary Fibrous Tumor of the Kidney Developing Local Recurrence. Case Rep Urol 2016; 2016: 2426874. DOI: 10.1155/2016/2426874
17. Sfoungaristos S, Papatheodorou M, Kavouras A et al. Solitary fibrous tumor of the kidney with massive retroperitoneal recurrence. A case presentation. Prague Med Rep 2012; 113(3): 246â50. DOI: 10.14712/23362936.2015.23
18. Llarena Ibarguren, Eizaguirre Zarzai B, Lecumberri CastaÃąos D, et al. Bilateral renal solitary fibrous tumor Arch Esp Urol 2003 Sep; 56 (7): 835â40.
19. Wu WW, Chu JT, Romansky SG, et al. Pediatric renal solitary fibrous tumor: report of a rare case and review of the literature. Int J Surg Pathol 2015 Feb; 23 (1): 34â47. DOI: 10.1177/1066896913492847
20. Khowaja A, Johnson-Rabbett B, Bantle J, et al. Hypoglycemia mediated by paraneoplastic production of Insulin like growth factor-2 from a malignant renal solitary fibrous tumor â clinical case and literature review. BMC Endocr Disord 2014 Jun 17; 14: 49. DOI: 10.1186/1472â6823â14â49
| Cikk ÃĐrtÃĐkelÃĐse | Eddig 1 felhasznÃĄlÃģ ÃĐrtÃĐkelte a cikket. |









HozzÃĄszÃģlÃĄsok